氧化还原中的几个概念
以下为《氧化还原中的几个概念》的无排版文字预览,完整格式请下载
下载前请仔细阅读文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
第三节:氧化还原反应 第3课时:氧化还原中的几个概念
旧知回顾
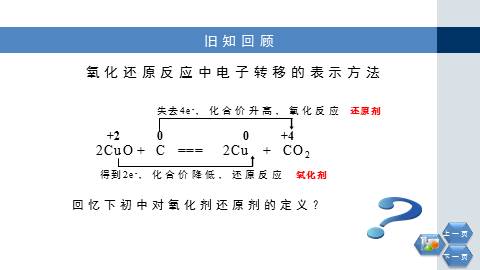
2CuO+ C === 2Cu + CO2
得到2e-,化合价降低,还原反应
+2
0
0
+4
失去4e-,化合价升高,氧化反应
氧化还原反应中电子转移的表示方法
氧化剂
还原剂
氧化剂:
得到电子(或电子对偏向)化合价降低的物质。
还原剂:
失去电子(或电子对偏离)化合价升高的物质。
新知讲解
针对反应物而言
被氧化:
还原剂发生的反应,反应中元素化合价升高
被还原:
氧化剂发生的反应,反应中元素化合价降低
新知讲解
注意:被氧化和被还原是针对元素而言
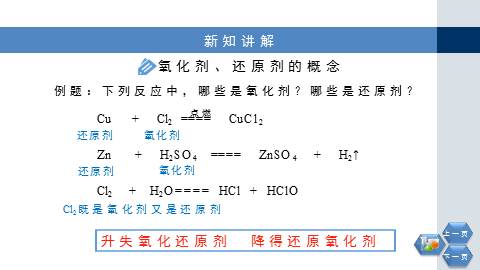
Cu + Cl2 ==== CuCl2
氧化剂
还原剂
氧化剂
还原剂
Cl2既是氧化剂又是还原剂
点燃
Zn + H2SO4 ==== ZnSO4 + H2↑
Cl2 + H2O==== HCl + HClO
例题:下列反应中,哪些是氧化剂?哪些是还原剂?
升失氧化还原剂 降得还原氧化剂
新知讲解
氧化性:
还原性:
物质得电子的性质,氧化剂具有氧化性, 物质得电子越容易,氧化性越强。
物质失电子的性质,还原剂具有还原性,物质失电子越容易,还原性越强。
新知讲解
氧化产物:
还原产物:
还原剂被氧化得到的产物
氧化剂被还原得到的产物
新知讲解
针对生成物而言
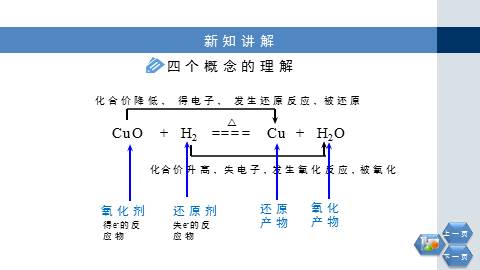
化合价降低,
得电子,
被还原
发生还原反应,
化合价升高,
失电子,
被氧化
发生氧化反应,
还原剂
得e-的反应物
失e-的反应物
新知讲解
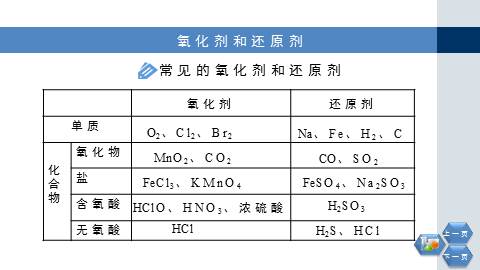
O2、Cl2、Br2
Na、Fe、H2、C
MnO2、CO2
CO、SO2
FeCl3、KMnO4
FeSO4、Na2SO3
HClO、HNO3、浓硫酸
H2SO3
HCl
H2S、HCl
氧化剂和还原剂
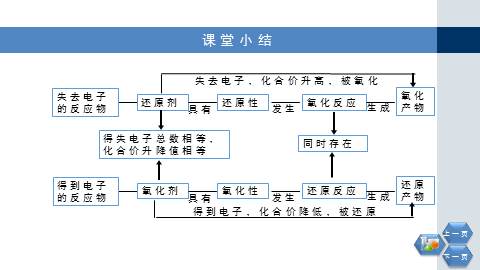
课堂小结
得失电子总数相等,化合价升降值相等
失去电子的反应物
同时存在
还原剂
还原性
具有
发生
氧化反应
氧化产物
生成
失去电子,化合价升高,被氧化
得到电子的反应物
氧化剂
氧化性
具有
发生
还原反应
还原产物
生成
得到电子,化合价降低,被还原
课堂小结
课堂练习
2.下列变化中,需要加入氧化剂才能实现的是( )
A.Cl-→Cl2 B.CuO→Cu
C.CaCO3→CO2 D.H2O2→O2
A
1.炼铁的反应:CO+FeO=CO2+Fe中,CO充当( )
A.氧化剂 B.还原剂
C.熔融剂 D.无法判断
B
课堂练习
3.以下说法中正确的是( )
A.物质所含元素化合价升高的反应叫做还原反应
B.在氧化还原反应中,失去电子的元素化合价降低
C.物质中某元素失去电子,则此物质是氧化剂
D.还原剂中必定有一种元素被氧化
D[全文已结束,注意以上仅为全文的文字预览,不包含图片和表格以及排版]
以上为《氧化还原中的几个概念》的无排版文字预览,完整格式请下载
下载前请仔细阅读上面文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
图片预览